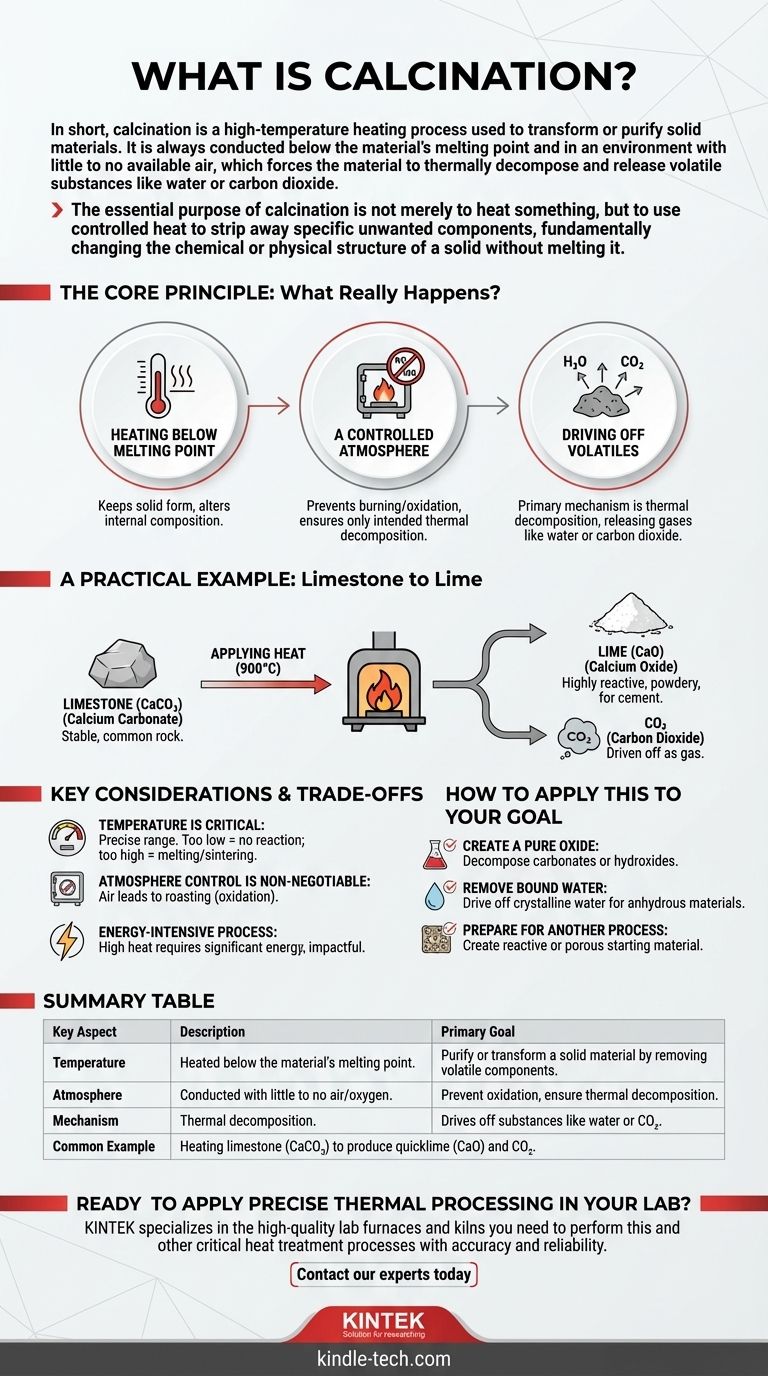
요약하자면, 소성은 고체 재료를 변환하거나 정제하는 데 사용되는 고온 가열 공정입니다. 이는 항상 재료의 녹는점 이하에서 공기 공급이 거의 없거나 전혀 없는 환경에서 수행되어 재료가 열분해되어 물이나 이산화탄소와 같은 휘발성 물질을 방출하도록 만듭니다.
소성의 본질적인 목적은 단순히 무언가를 가열하는 것이 아니라, 제어된 열을 사용하여 특정 원치 않는 구성 요소를 제거하고 재료를 녹이지 않으면서 고체의 화학적 또는 물리적 구조를 근본적으로 변화시키는 것입니다.
핵심 원리: 소성 중에 실제로 일어나는 일은 무엇인가요?
소성을 이해하려면 단순한 가열 행위 이상을 살펴보는 것이 중요합니다. 이 공정은 정확한 결과를 얻기 위해 함께 작용하는 세 가지 특정 조건으로 정의됩니다.
녹는점 이하의 가열
목표는 고체 재료 자체 내에서 화학적 또는 물리적 변화를 유도하는 것입니다. 온도를 녹는점 이하로 유지함으로써 재료의 내부 구성은 변경되지만 전반적인 고체 형태는 유지됩니다.
제어된 분위기
소성은 공기(산소)가 없거나 매우 제한적으로 공급되는 상태에서 수행됩니다. 이것은 결정적인 차이점입니다. 재료가 연소되거나 산화되는 것을 방지하여 의도된 열분해 반응만 일어나도록 보장합니다.
휘발성 물질의 제거
주요 메커니즘은 열분해입니다. 가해진 열은 화학 결합을 끊는 데 필요한 에너지를 제공하여 재료가 휘발성 부분(일반적으로 물(H₂O) 또는 이산화탄소(CO₂)와 같이 기체가 될 수 있는 물질)을 방출하도록 만듭니다.

실제 예시: 석회석에서 생석회로
소성의 가장 일반적이고 이해하기 쉬운 예는 시멘트 산업용 생석회 생산에서의 역할입니다.
시작 재료: 석회석
이 공정은 화학적으로 탄산칼슘(CaCO₃)으로 알려진 석회석으로 시작됩니다. 이는 안정적인 일반 암석입니다.
공정: 열 가하기
석회석을 대형 가마에서 약 900°C(1650°F)의 온도로 가열합니다. 이 고온은 탄산칼슘을 분해합니다.
최종 생성물: 생석회와 CO₂
소성 공정은 이산화탄소(CO₂)를 기체로 방출하고 반응성이 높은 분말 형태의 산화칼슘(CaO), 즉 생석회를 남깁니다. 이 결과로 생성된 생석회는 시멘트 및 기타 산업 응용 분야의 기본 재료입니다.
주요 고려 사항 및 상충 관계
소성은 강력하지만 정밀함이 요구되는 공정입니다. 핵심 요구 사항을 잘못 이해하면 실패하거나 비효율적인 결과가 나올 수 있습니다.
온도가 중요합니다
이 공정은 특정 온도 범위 내에서 작동합니다. 온도가 너무 낮으면 분해 반응이 일어나지 않습니다. 너무 높으면 재료가 녹거나 소결(sinter, 고체 덩어리로 융합)될 수 있으며, 이는 최종 응용 분야에 바람직하지 않을 수 있습니다.
분위기 제어는 필수입니다
가마에 제어되지 않은 공기가 유입되면 공정 전체가 바뀝니다. 예를 들어, 금속 황화물을 공기 존재 하에 가열하는 것을 배소(roasting)라고 하며, 이는 소성과는 완전히 다른 결과를 가져오는 산화 공정입니다.
에너지 집약적인 공정입니다
막대한 양의 재료를 그렇게 높은 온도로 가열하려면 상당한 양의 에너지가 필요합니다. 이로 인해 소성은 모든 산업 작업 흐름에서 비용이 많이 들고 환경에 영향을 미치는 단계가 됩니다.
목표에 적용하는 방법
소성을 언제 그리고 왜 사용해야 하는지 이해하는 것이 재료 과학, 화학 및 엔지니어링에서 이를 효과적으로 활용하는 열쇠입니다.
- 순수한 산화물 생성에 중점을 두는 경우: 소성은 탄산염(석회석과 같은) 또는 수산화물을 분해하여 해당 산화물을 생성하는 확실한 방법입니다.
- 결합된 물 제거에 중점을 두는 경우: 이 공정은 수화된 광물에서 결정수를 제거하여 무수(물 없는) 형태의 재료를 만드는 데 사용됩니다.
- 다른 공정을 위한 재료 준비에 중점을 두는 경우: 소성은 후속 화학 반응을 위해 더 반응성이 높거나 다공성인 시작 재료를 만드는 데 종종 중요한 준비 단계입니다.
궁극적으로 소성은 제어된 열을 사용하여 고체를 정제하고 변형시키는 정밀한 산업 도구입니다.
요약표:
| 핵심 측면 | 설명 |
|---|---|
| 주요 목표 | 휘발성 성분을 제거하여 고체를 정제하거나 변환합니다. |
| 온도 | 재료의 녹는점 이하로 가열합니다. |
| 분위기 | 산화를 방지하기 위해 공기/산소 공급이 거의 또는 전혀 없는 상태에서 수행됩니다. |
| 메커니즘 | 열분해가 물 또는 CO₂와 같은 물질을 방출합니다. |
| 일반적인 예 | 석회석(CaCO₃)을 가열하여 생석회(CaO)와 CO₂를 생성합니다. |
실험실에서 정밀한 열처리를 적용할 준비가 되셨나요?
소성은 순수한 산화물을 만들고, 물을 제거하고, 반응성 재료를 준비하기 위한 기본 단계입니다. KINTEK은 정확하고 안정적으로 이 공정 및 기타 중요한 열처리 공정을 수행하는 데 필요한 고품질 실험실로와 가마를 전문으로 합니다.
귀하의 실험실의 특정 재료 및 목표에 맞는 완벽한 소성 솔루션을 찾으려면 지금 전문가에게 문의하십시오.
시각적 가이드