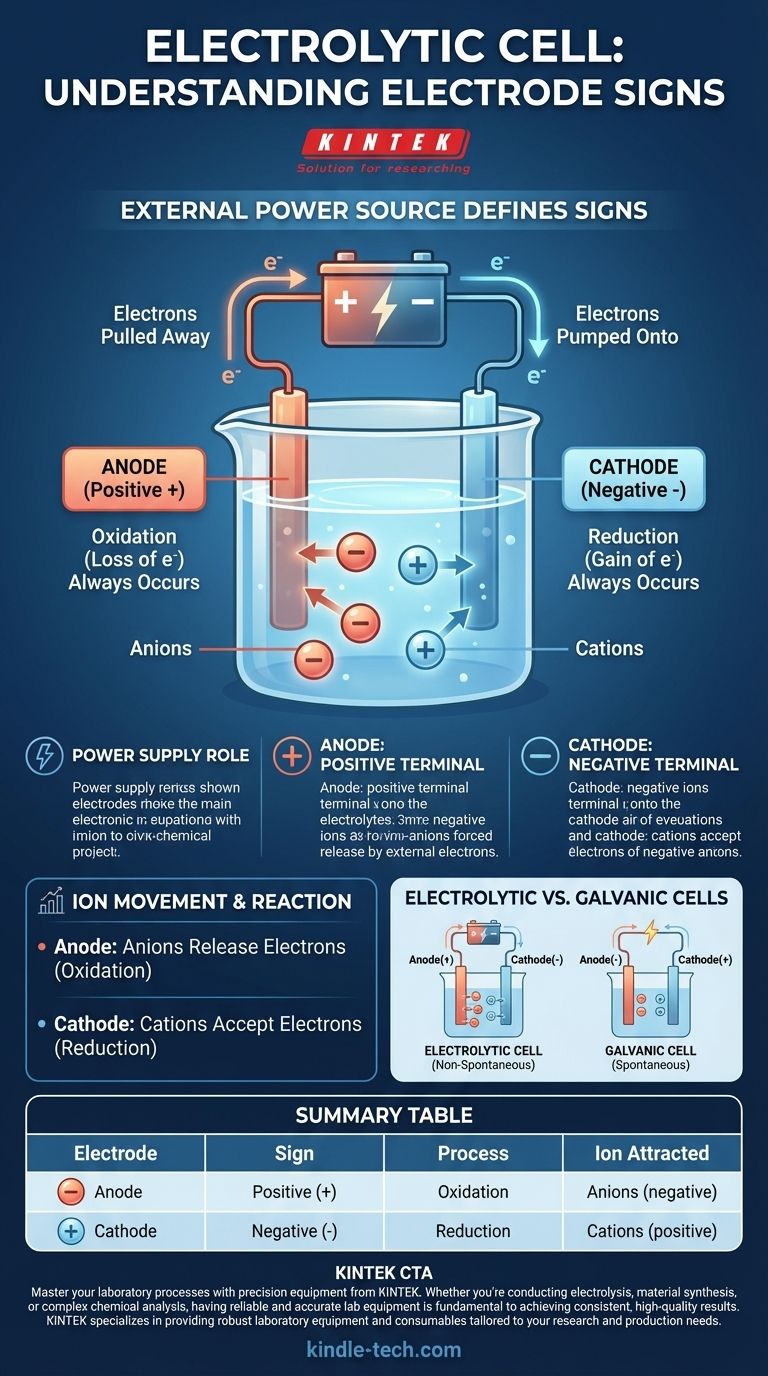
전해 전지에서 부호 규칙은 외부 전원에 의해 정의됩니다. 양극에는 양극(+) 부호가 할당되고, 음극에는 음극(-) 부호가 할당됩니다. 이는 자발적으로 발생하지 않는 화학 반응을 구동하기 위해 외부 전압이 인가되기 때문입니다.
전해 전지를 이해하는 핵심은 전해 전지가 독립적인 시스템이 아니라는 것을 인식하는 것입니다. 전극의 부호는 연결된 외부 전원 공급 장치에 의해 전적으로 결정되며, 비자발적인 화학 변화를 강제로 발생시킵니다.
외부 전원이 부호를 정의하는 이유
전해 전지는 전기 에너지를 사용하여 화학 에너지를 생성합니다. 전기 분해라고 알려진 이 과정은 반응을 시작하고 유지하기 위해 외부 힘(배터리 또는 DC 전원 공급 장치)을 필요로 합니다.
전원 공급 장치의 역할
전원 공급 장치는 "전자 펌프" 역할을 합니다. 한 전극에서 전자를 끌어당겨 다른 전극으로 밀어 넣어 전하 불균형을 생성하고 전해액 용액의 이온이 반응하도록 강제합니다.
양극은 양극 단자에 연결됩니다
외부 전원 공급 장치의 양극 단자는 양극에 연결됩니다. 이 단자는 양극에서 전자를 적극적으로 끌어당겨 양극에 순 양전하를 남깁니다.
음극은 음극 단자에 연결됩니다
반대로, 전원 공급 장치의 음극 단자는 음극에 연결됩니다. 이 단자는 음극으로 전자를 적극적으로 펌핑하여 음극에 과도한 전자를 공급하고 순 음전하를 부여합니다.

이온 이동이 반응을 생성하는 방법
전극에 강제로 가해진 전하는 전해액에 용해된 이온을 끌어당겨 이동하고 반응하도록 만듭니다. 산화 및 환원의 기본 정의는 일정하게 유지됩니다.
양극: 산화가 일어나는 곳 (항상)
전지 유형에 관계없이 산화(전자를 잃는 것)는 항상 양극에서 발생합니다. 전해 전지에서는 음전하를 띤 이온(음이온)이 양극으로 끌려가 과도한 전자를 방출하고 산화됩니다.
음극: 환원이 일어나는 곳 (항상)
마찬가지로 환원(전자를 얻는 것)은 항상 음극에서 발생합니다. 용액의 양전하를 띤 이온(양이온)은 음극으로 끌려가 과도한 전자를 받아 환원됩니다.
중요한 구분: 전해 전지 대 갈바니 전지
혼란의 주요 원인은 전해 전지와 갈바니(또는 볼타) 전지(예: 표준 배터리)를 비교할 때 발생합니다. 이들의 부호 규칙은 매우 구체적인 이유로 반대입니다.
자발적 반응 대 비자발적 반응
갈바니 전지는 자발적인 화학 반응에 의해 작동하며 전기 에너지를 생산합니다. 여기서는 양극이 전자의 자연적인 원천이 되어 음극이 되고, 음극은 전자가 소비되는 곳이 되어 양극이 됩니다.
전해 전지는 비자발적인 반응을 일으켜 전기 에너지를 소비합니다. 외부 전원은 반응이 진행되도록 자연적인 극성을 반전시킵니다.
보편적인 상수
부호의 차이에도 불구하고 두 전지 유형 모두에서 핵심 과정은 동일합니다.
- 양극은 항상 산화가 일어나는 곳입니다.
- 음극은 항상 환원이 일어나는 곳입니다.
부호를 기억하는 방법
목표에 따라 규칙을 명확하게 유지하려면 다음 원칙을 사용하십시오.
- 주요 초점이 단자를 식별하는 경우: 전해 전지에서 부호는 외부 전원 공급 장치와 일치한다는 것을 기억하십시오. 양극은 양극이고 음극은 음극입니다.
- 주요 초점이 이온을 추적하는 경우: 음전하를 띤 음이온은 양극으로 이동하고, 양전하를 띤 양이온은 음극으로 이동한다는 간단한 반대 전하 규칙을 따르십시오.
- 주요 초점이 전지 유형을 구별하는 경우: "전해"를 외부 전원 공급 장치와 연결하여 반응을 구동하기 위해 양극에 양전하를, 음극에 음전하를 강제합니다.
궁극적으로 전해 전지의 부호는 화학 반응의 자연적인 흐름을 무시하는 외부 전원 공급 장치의 직접적인 결과입니다.
요약표:
| 전극 | 부호 | 과정 | 끌어당기는 이온 |
|---|---|---|---|
| 양극 | 양극 (+) | 산화 | 음이온 (음전하) |
| 음극 | 음극 (-) | 환원 | 양이온 (양전하) |
KINTEK의 정밀 장비로 실험실 프로세스를 마스터하십시오.
전기 분해, 재료 합성 또는 복잡한 화학 분석을 수행하든 관계없이 신뢰할 수 있고 정확한 실험실 장비는 일관되고 고품질의 결과를 얻는 데 필수적입니다. KINTEK은 연구 및 생산 요구 사항에 맞춰 견고한 실험실 장비 및 소모품을 제공하는 데 특화되어 있습니다.
오늘 전문가에게 문의하여 당사의 솔루션이 귀하의 혁신을 강화하고 실험실 워크플로우의 효율성을 높이는 방법에 대해 논의하십시오.
시각적 가이드