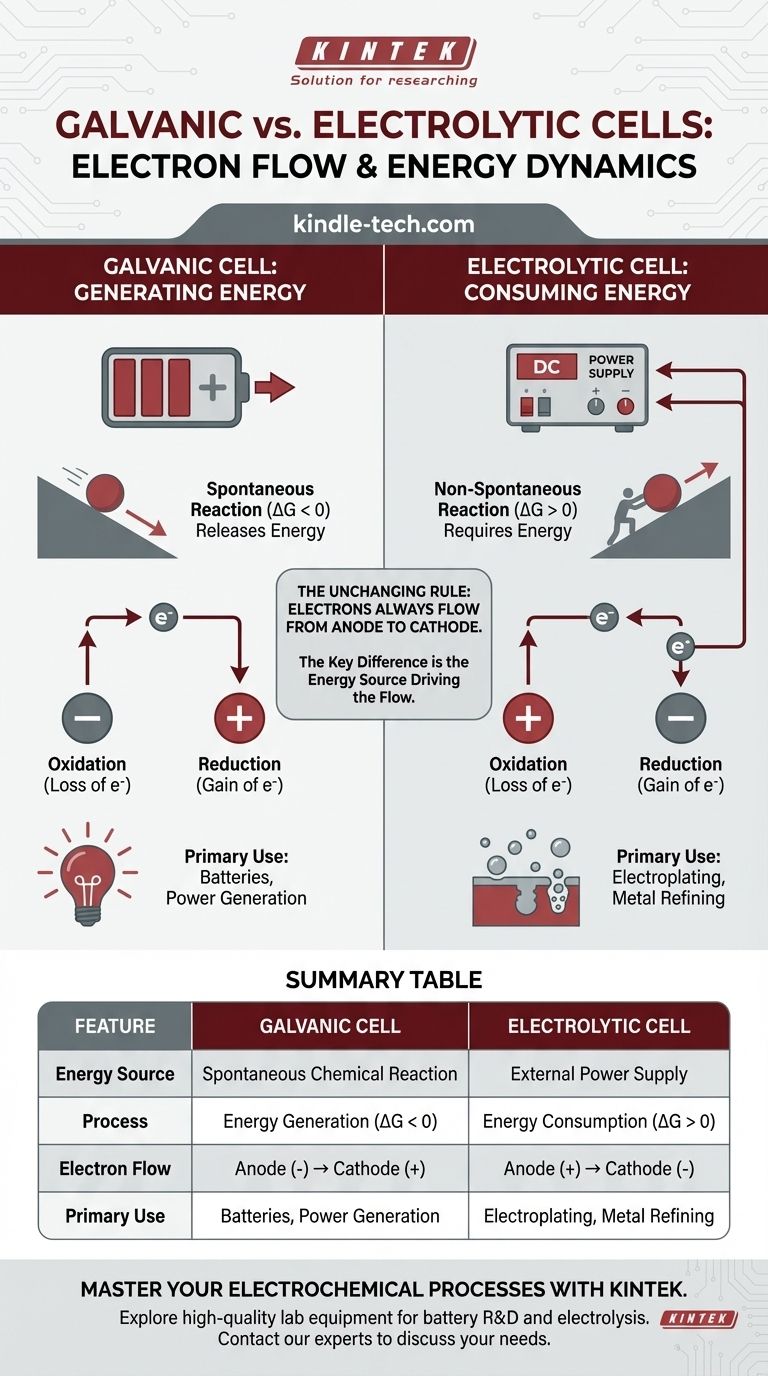
모든 전기화학 전지에서 외부 회로의 전자 흐름은 항상 양극(anode)에서 음극(cathode)으로 향합니다. 결정적인 차이점은 전자가 흐르는 이유에 있습니다. 갈바니 전지에서는 자발적인 화학 반응이 에너지를 생성하여 전자를 밀어냅니다. 전기분해 전지에서는 외부 전원 공급 장치가 에너지를 제공하여 전자의 흐름을 강제하고 비자발적인 반응을 구동합니다.
근본적인 차이점은 산화 및 환원과 관련하여 전자 흐름의 방향이 아니라, 과정을 구동하는 에너지원입니다. 갈바니 전지는 저장된 화학 에너지를 전기 에너지로 변환하는 반면, 전기분해 전지는 외부 전기 에너지를 사용하여 화학적 변화를 강제합니다.

핵심 원리: 자발적 반응 대 비자발적 반응
전자 흐름을 이해하려면 먼저 전지의 에너지 역학을 이해해야 합니다. 전체 시스템은 화학 반응이 스스로 발생하는지 아니면 강제되어야 하는지에 따라 결정됩니다.
갈바니 전지: 에너지 생성
갈바니 전지(볼타 전지라고도 함)는 자발적인 화학 반응을 활용합니다. 이것은 공을 아래로 굴리는 것과 같아서 과정이 자연스럽게 에너지를 방출합니다.
이 자발적인 반응은 음의 깁스 자유 에너지(ΔG < 0)를 가집니다. 이 화학 에너지의 방출은 직접 전기 에너지로 변환되어 양극에서 외부 회로를 통해 음극으로 전자를 밀어냅니다.
갈바니 전지는 모든 기존 배터리의 기반입니다.
전기분해 전지: 에너지 소비
전기분해 전지는 비자발적인 화학 반응을 구동하는 데 사용됩니다. 이것은 공을 위로 밀어 올리는 것과 같아서 일어나기 위해 지속적인 외부 에너지 투입이 필요합니다.
이 반응은 양의 깁스 자유 에너지(ΔG > 0)를 가집니다. 배터리나 전원 공급 장치와 같은 외부 전원 공급 장치는 "전자 펌프" 역할을 합니다. 이는 전자를 음극에 강제로 공급하고 양극에서 전자를 끌어내어 스스로 일어나지 않을 반응을 구동합니다.
전자 흐름 및 전극 극성 분석
전자 흐름에 대한 혼란은 종종 전극의 변화하는 극성에서 비롯됩니다. 양극과 음극의 역할은 고정되어 있지만, 그 전하는 그렇지 않습니다.
불변의 규칙: 양극에서 음극으로
정의에 따르면 산화(전자 손실)가 일어나는 곳은 항상 양극이며, 환원(전자 획득)이 일어나는 곳은 항상 음극입니다.
양극에서 전자가 손실되고 음극에서 전자가 얻어지므로 외부 전선에서 전자는 항상 양극에서 음극으로 흐릅니다. 이는 두 전지 유형 모두에 대한 보편적인 상수입니다.
결정적인 차이: 전극 전하
두 전지 유형 간에 전극의 극성(양 또는 음 전하)이 바뀌는 것이 대부분의 혼란의 원인입니다.
갈바니 전지에서 양극은 전자를 방출하는 자발적인 산화 부위입니다. 이 음전하 축적으로 인해 양극은 음(-) 단자가 됩니다. 전자를 소비하는 음극은 양(+) 단자이 됩니다.
전기분해 전지에서는 외부 전원 공급 장치가 극성을 결정합니다. 이는 전자를 강제로 공급하여 환원을 구동하기 위해 셀의 음극에 자체 음극 단자를 연결합니다. 이는 산화를 구동하기 위해 전자를 끌어내기 위해 셀의 양극에 자체 양극 단자를 연결합니다.
- 갈바니 전지: 양극 (-) → 음극 (+)
- 전기분해 전지: 양극 (+) → 음극 (-)
실제 응용 이해하기
에너지 변환(energy conversion)의 근본적인 차이점은 이러한 전지가 어떻게 사용되는지를 결정합니다. 하나는 전력을 생산하고 다른 하나는 귀중한 물질을 생산하기 위해 전력을 소비합니다.
갈바니 전지: 필요할 때 전력 공급
갈바니 전지의 주요 이점은 휴대용 전기 에너지원으로 작동할 수 있다는 것입니다.
이것들은 간단한 AA 전지부터 자동차 배터리까지 모든 배터리의 기초입니다. 주요 한계는 화학 반응물이 결국 소모되어 전압이 떨어지고 배터리가 방전된다는 것입니다.
전기분해 전지: 화학적 변화 강제
전기분해 전지의 목적은 전기를 사용하여 화학 제품을 만드는 것입니다.
전기분해라고 하는 이 과정은 금속 정제(예: 순수 알루미늄 생산), 표면을 보호 금속층으로 도금, 물을 수소와 산소로 분해하는 것과 같은 산업 응용 분야에 필수적입니다. 단점은 지속적이고 종종 비용이 많이 드는 전기 에너지 공급이 필요하다는 것입니다.
목표에 적용하는 방법
귀하의 접근 방식은 전기를 생성해야 하는지 또는 화학 반응을 구동해야 하는지에 전적으로 달려 있습니다.
- 전력 생성 또는 배터리 만들기가 주요 초점인 경우: 자발적인 반응이 전류를 생성하는 갈바니 전지를 다루고 있는 것입니다.
- 금속 정제, 표면 도금 또는 화합물 분해가 주요 초점인 경우: 비자발적인 반응을 구동하기 위해 외부 전력을 사용하는 전기분해 전지가 필요합니다.
- 핵심 원리 이해가 주요 초점인 경우: 산화는 항상 양극에서 일어나고 환원은 음극에서 일어난다는 것을 기억하십시오. 핵심 차이점은 반응이 자발적인지(갈바니) 아니면 강제적인지(전기분해)입니다.
자발적인 에너지 방출과 강제적인 에너지 입력 사이의 이러한 구별을 이해하는 것이 전기화학 전지를 마스터하는 열쇠입니다.
요약표:
| 특징 | 갈바니 전지 | 전기분해 전지 |
|---|---|---|
| 에너지원 | 자발적 화학 반응 | 외부 전원 공급 장치 |
| 과정 | 에너지 생성 (ΔG < 0) | 에너지 소비 (ΔG > 0) |
| 전자 흐름 | 양극 (-) → 음극 (+) | 양극 (+) → 음극 (-) |
| 주요 용도 | 배터리, 전력 생성 | 전기 도금, 금속 정제 |
KINTEK과 함께 전기화학 공정을 마스터하세요
새로운 배터리 기술을 개발하든 전기분해를 통해 재료를 정제하든 정확하고 신뢰할 수 있는 결과를 얻으려면 올바른 실험실 장비가 중요합니다. KINTEK은 모든 전기화학 연구 개발에 필요한 정확한 도구를 제공하는 고품질 실험실 장비 및 소모품을 전문으로 합니다.
귀하의 연구실이 성공할 수 있도록 장비를 갖추도록 도와드리겠습니다. 지금 바로 전문가에게 문의하여 귀하의 특정 요구 사항에 대해 논의하고 KINTEK이 귀하의 획기적인 연구를 어떻게 지원할 수 있는지 알아보십시오.
시각적 가이드