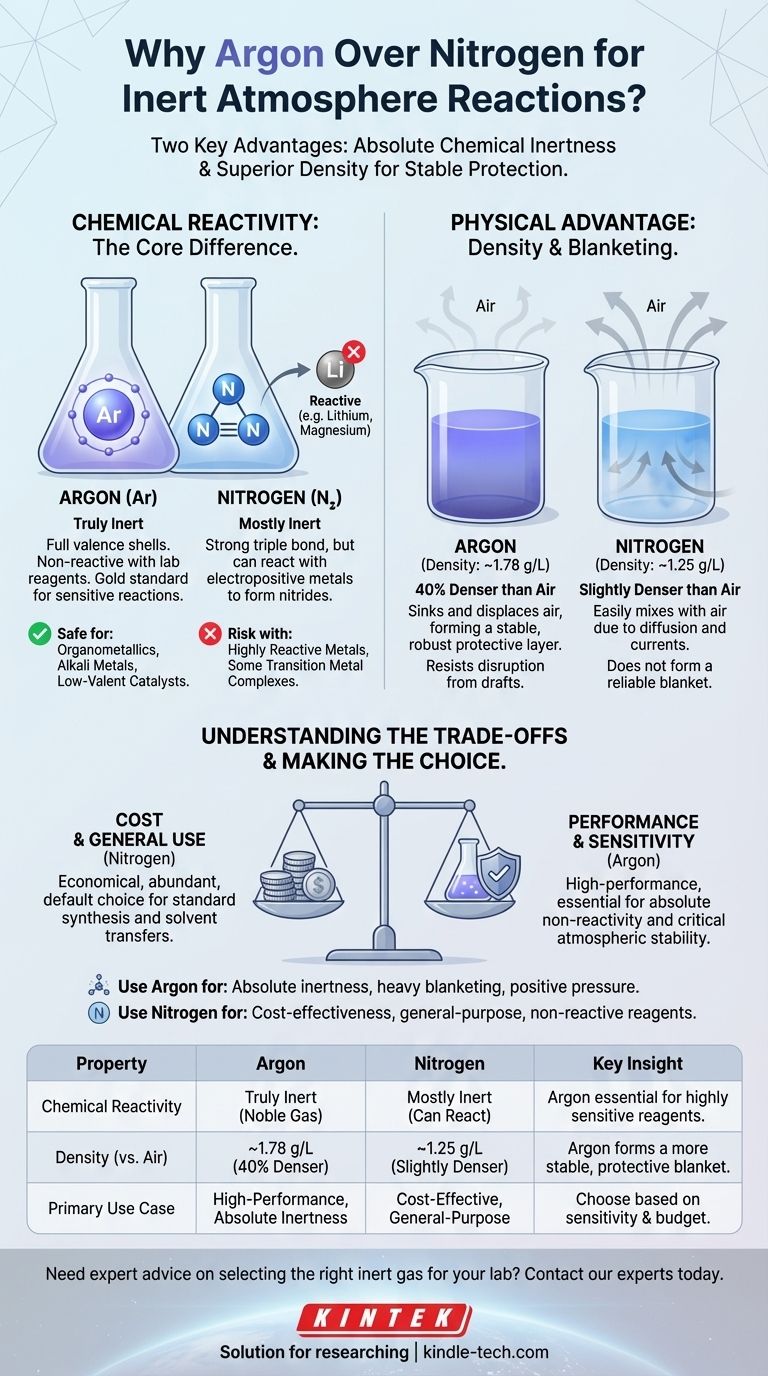
실제로 아르곤은 두 가지 주요 특성 때문에 불활성 분위기 반응에 질소보다 "더 좋다"고 종종 간주됩니다. 아르곤은 실험실 시약과 반응할 수 없는 진정한 불활성 비활성 기체인 반면, 질소는 특정 조건에서 반응할 수 있습니다. 또한 아르곤의 높은 밀도는 반응물 위에 더 안정적이고 보호적인 "담요"를 형성하여 공기를 더 효과적으로 밀어낼 수 있도록 합니다.
아르곤과 질소 중 어느 것이 보편적으로 더 나은지에 대한 선택이 아니라, 특정 작업에 어떤 것이 더 적합한지에 대한 문제입니다. 질소는 일반적인 불활성화를 위한 경제적인 일꾼인 반면, 아르곤은 절대적인 비반응성과 대기 안정성을 요구하는 반응을 위한 고성능 옵션입니다.

핵심 차이: 화학적 반응성
한 기체를 다른 기체보다 선택하는 가장 근본적인 이유는 반응에 참여할 가능성 때문입니다.
아르곤: 불활성의 정의
아르곤은 비활성 기체입니다. 원자가 전자 껍질이 완전히 채워져 있어 사실상 모든 실험실 조건에서 매우 안정적이고 비반응성입니다.
화학자에게 이것은 황금 표준입니다. 시약이 아무리 민감하더라도 아르곤이 반응을 방해하지 않을 것이라고 확신할 수 있습니다.
질소: "거의" 불활성
질소 가스(N₂)는 매우 강한 삼중 결합으로 연결된 두 개의 질소 원자로 구성됩니다. 이 결합은 끊는 데 많은 에너지가 필요하므로 N₂는 대부분 불활성이며 많은 응용 분야에 잘 사용됩니다.
그러나 완전히 비반응성은 아닙니다. 특히 리튬, 마그네슘 및 일부 전이 금속 착물과 같은 전기 양성 금속과 같은 고반응성 시약은 N₂와 반응하여 금속 질화물을 형성할 수 있습니다. 이 원치 않는 부반응은 수율을 감소시키거나 불순물을 유발할 수 있습니다.
물리적 이점: 밀도
화학적 반응성 외에도 실험실에서 기체의 물리적 거동은 중요한 요소입니다. 공기는 기체 혼합물이지만, 우리가 비교할 수 있는 평균 밀도를 가지고 있습니다.
- 아르곤 밀도: ~1.78 g/L
- 공기 밀도: ~1.23 g/L
- 질소 밀도: ~1.25 g/L
밀도가 보호 "담요"를 만드는 방법
아르곤은 공기보다 약 40% 더 밀도가 높습니다. 플라스크를 아르곤으로 퍼지하면, 아르곤은 효과적으로 가라앉아 더 가벼운 공기를 밀어내고 위로 밀어냅니다. 그런 다음 반응 혼합물 위에 자리 잡아 안정적이고 무거운 담요를 형성하여 방해에 저항합니다.
반면에 질소는 공기보다 약간만 밀도가 높습니다. 확산과 방의 미세한 기류 또는 대류로 인해 공기와 섞일 가능성이 훨씬 더 큽니다. 동일한 강력한 보호층을 형성하지 않습니다.
실험실 설정에 대한 실제적 의미
이 밀도 차이는 실제적인 결과를 가져옵니다. 글러브 박스나 슐렌크 라인에서 아르곤의 양압은 더 관대한 분위기를 제공합니다. 작은 누출이 발생하면 밀도가 높은 아르곤이 우선적으로 흘러나와 더 가벼운 공기가 유입되는 것을 방지합니다.
많은 전기화학 실험에서와 같이 개방형 용기를 덮는 데 의존하는 기술의 경우, 아르곤은 용액 위에 안정적으로 유지되므로 훨씬 우수합니다. 질소는 주변 공기와 거의 즉시 섞일 것입니다.
상충 관계 이해하기
이상적인 기체를 선택하려면 성능과 실제적인 제약 사이의 균형을 맞춰야 합니다.
비용: 많은 사람들에게 결정적인 요소
질소는 지구 대기의 약 78%를 차지하는 반면, 아르곤은 1% 미만입니다. 이러한 풍부함의 차이로 인해 질소는 생산 및 구매 비용이 훨씬 저렴합니다.
극도의 불활성이 필요하지 않은 대규모 산업 공정 또는 일상적인 실험실 절차의 경우, 질소 사용으로 인한 비용 절감은 상당하며 종종 기본 선택이 됩니다.
반응성: "거의" 불활성이 충분할 때
질소의 잠재적 반응성은 화학 시스템이 N≡N 삼중 결합을 끊을 수 있는 경우에만 중요합니다.
대부분의 유기 반응, 정제 및 용매 이동의 경우 질소는 완벽하게 적절합니다. 시약은 질화물을 형성할 만큼 충분히 반응성이 없으므로 아르곤은 불필요한 비용입니다.
반응에 적합한 선택하기
화학 절차의 특정 요구 사항과 실험실의 실제 상황을 바탕으로 결정하십시오.
- 민감한 시약에 대한 절대적인 불활성이 주요 초점인 경우: 유기 금속 화합물(특히 Li, Mg 포함), 알칼리 금속, 저가 전이 금속 촉매 또는 질화물 형성이 알려진 위험인 모든 시스템으로 작업할 때 아르곤을 사용하십시오.
- 비용 효율성과 범용 사용이 주요 초점인 경우: 대부분의 표준 유기 합성, 용매 증류, 재결정화 및 극도로 반응성이 높은 종을 포함하지 않는 기타 절차에 질소를 사용하십시오.
- 안정적인 분위기 유지가 주요 초점인 경우: 전기화학과 같이 무거운 기체 담요가 필요한 기술이나 잠재적 누출에 대한 양압 유지가 중요한 설정에서 아르곤을 사용하십시오.
궁극적으로 각 기체의 독특한 화학적 및 물리적 특성을 이해하면 실험에 가장 정보에 입각하고 경제적인 선택을 할 수 있습니다.
요약 표:
| 특성 | 아르곤 | 질소 | 핵심 통찰 |
|---|---|---|---|
| 화학적 반응성 | 진정한 불활성 (비활성 기체) | 대부분 불활성, 그러나 전기 양성 금속과 반응할 수 있음 | 아르곤은 매우 민감한 시약에 필수적입니다. |
| 밀도 (vs. 공기) | ~1.78 g/L (40% 더 밀도가 높음) | ~1.25 g/L (약간 더 밀도가 높음) | 아르곤은 더 안정적이고 보호적인 담요를 형성합니다. |
| 주요 사용 사례 | 절대적인 불활성을 요구하는 고성능 반응 | 범용 불활성화를 위한 비용 효율적인 솔루션 | 반응의 민감도와 예산에 따라 선택하십시오. |
특정 실험실 응용 분야에 적합한 불활성 기체 선택에 대한 전문가의 조언이 필요하십니까?
KINTEK은 민감한 반응이 완벽하게 보호되도록 아르곤 및 질소 시스템을 포함한 고순도 실험실 가스 및 장비 제공을 전문으로 합니다. 저희 팀은 최대 수율과 안전을 위해 설정을 최적화하는 데 도움을 드릴 수 있습니다.
오늘 저희 전문가에게 연락하여 불활성 분위기 요구 사항을 논의하고 실험실에 가장 효율적인 솔루션을 찾으십시오.
시각적 가이드
관련 제품
- 다양한 과학적 응용 분야를 위한 맞춤형 실험실 고온 고압 반응기
- 수열 합성용 고압 실험실 오토클브 반응기
- 실험실용 미니 스테인리스강(SS) 고압 오토클레이브 반응기
- 고급 과학 및 산업 응용 분야를 위한 맞춤형 고압 반응기
- 스테인리스 고압 오토클레이브 반응기 실험실 압력 반응기



















