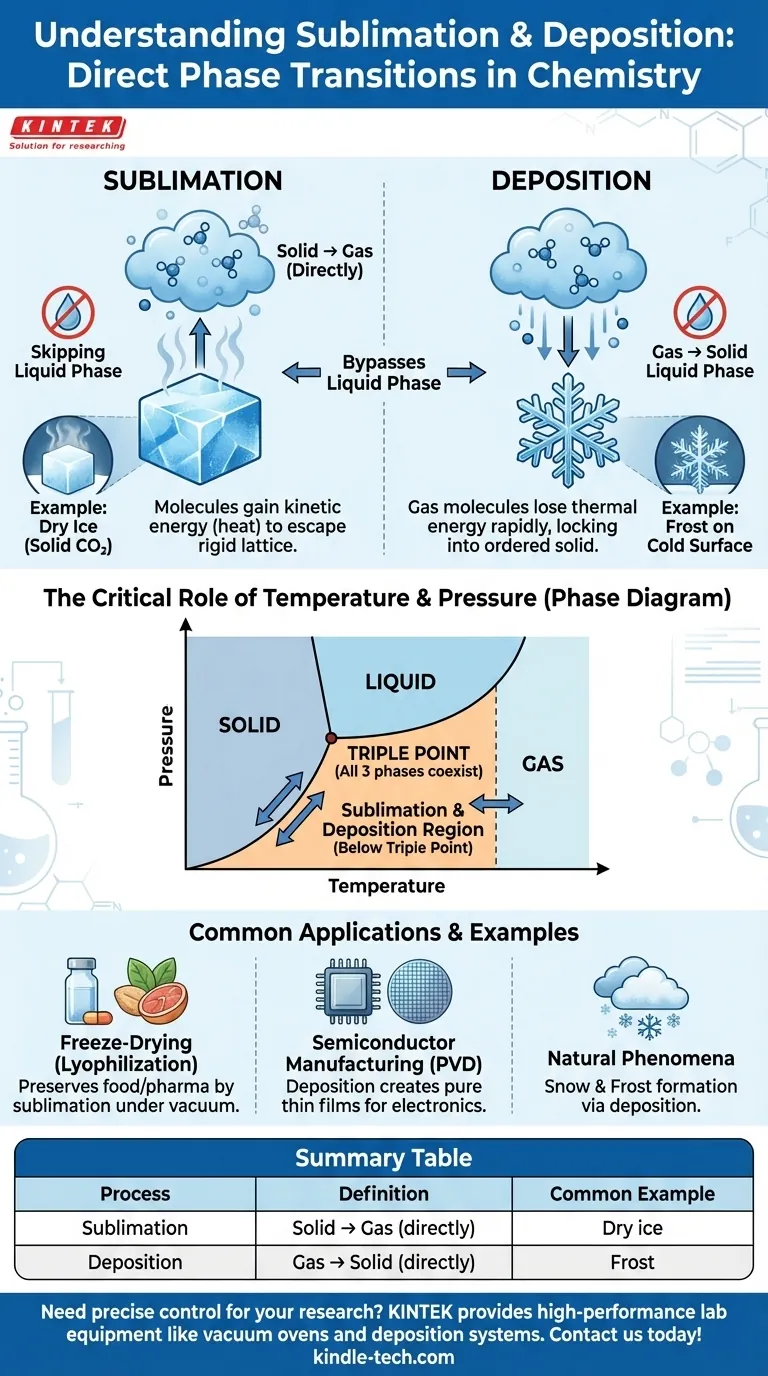
물질의 연구에서, 승화(sublimation)와 증착(deposition)은 물질이 액체 상태를 완전히 건너뛰고 고체 상태와 기체 상태 사이를 직접 전환하는 상 변화입니다. 승화는 고체가 기체로 직접 변환되는 것입니다. 증착은 그 반대 과정으로, 기체가 직접 고체로 변하는 것입니다.
이해해야 할 핵심 원리는 승화와 증착이 동전의 양면이라는 것입니다. 이는 특정 온도와 압력 조건에서 액체 상태를 건너뛰고 고체상과 기체상 사이의 직접적인 양방향 경로를 나타냅니다.
상 변화의 메커니즘
물질이 액체 상을 건너뛰는 이유를 이해하려면 분자의 에너지와 배열을 살펴봐야 합니다. 상 변화는 근본적으로 분자 에너지와 운동 자유도의 변화에 관한 것입니다.
승화: 고체에서 기체로의 전환
고체 상태에서 분자들은 고정된, 종종 결정 구조에 갇혀 있지만 여전히 제자리에서 진동합니다.
에너지(주로 열의 형태)가 추가되면 이러한 진동이 증가합니다. 승화 시 분자들은 고정된 격자 구조에 묶어 두는 분자 간 힘을 극복할 만큼 충분한 운동 에너지를 얻어 직접 기체로 빠져나갑니다.
고전적인 예는 드라이아이스, 즉 고체 이산화탄소입니다. 상온 및 표준 압력에서 액체 웅덩이가 되지 않고 직접 기체 이산화탄소로 변합니다.
증착: 기체에서 고체로의 전환
증착은 승화와 반대입니다. 이는 기체 상태의 분자들이 열에너지를 빠르게 잃을 때 발생합니다.
이러한 급격한 에너지 손실로 인해 빠르게 움직이는 기체 분자들이 너무 느려져 액체로 응축될 기회 없이 직접 정렬된 고체 구조 속으로 잠깁니다.
차가운 창문에 서리가 맺히는 것이 완벽한 예입니다. 공기 중의 수증기가 영하의 표면에 닿으면 직접 얼음 결정으로 변합니다.

온도와 압력의 결정적인 역할
물질이 승화할지, 녹을지, 끓을지는 물질 자체의 고유한 특성만으로 결정되지 않습니다. 이는 상 다이어그램에서 가장 잘 시각화되는 외부 온도 및 압력 조건에 의해 결정됩니다.
삼중점 소개
모든 물질에는 삼중점(triple point)이라고 불리는 특정 온도와 압력의 조합이 있습니다. 이는 고체, 액체, 기체 상이 열역학적 평형 상태에서 공존할 수 있는 고유한 지점입니다.
액체 상을 건너뛰는 이유
승화와 증착은 삼중점보다 낮은 온도 및 압력 조합에서 발생합니다.
이러한 낮은 압력에서는 액체 상이 안정적이지 않습니다. 고체에 에너지를 추가하면 고체가 직접 기체 상의 경계로 밀려나고(승화), 기체에서 에너지를 제거하면 기체가 직접 고체 상으로 넘어가게 됩니다(증착).
일반적인 응용 및 예시
이러한 과정은 단순한 이론적 개념이 아니라 자연 현상과 중요한 산업 기술 모두의 중심에 있습니다.
작동 중인 승화: 동결 건조
동결 건조(승화 건조)는 식품 및 의약품을 보존하는 주요 방법입니다. 물질을 먼저 얼린 다음 주변 압력을 극적으로 낮추면 얼어붙은 물(얼음)이 물 증기로 승화되어 열 손상 없이 제품을 건조하게 만듭니다.
기술에서의 증착: 반도체 제조
기술 산업에서는 물리 기상 증착(PVD)이라는 공정을 사용하여 박막을 만듭니다. 고체 물질을 진공 상태에서 기화시키고, 생성된 기체가 컴퓨터 칩 제작에 사용되는 실리콘 웨이퍼와 같은 기판 위에 순수한 고체 필름으로 증착됩니다.
자연 현상: 눈과 서리
구름 속에서 눈이 형성되는 것은 증착의 자연적인 예입니다. 대기 중의 수증기가 냉각되어 복잡한 얼음 결정으로 직접 증착되어 액체 빗방울로 존재한 적이 없는 눈송이를 형성합니다.
목표에 맞는 올바른 선택하기
이러한 개념을 이해하면 자연 및 산업 공정을 더 명확하게 해석할 수 있습니다.
- 일상적인 현상을 시각화하는 데 중점을 둔다면: 드라이아이스가 "연기"를 내는 것은 승화이며, 추운 아침 잔디밭에 서리가 맺히는 것은 증착임을 기억하세요.
- 산업 공정 이해에 중점을 둔다면: 동결 건조는 물을 부드럽게 제거하기 위해 승화를 사용하며, 첨단 전자 장치를 만드는 것은 종종 층별로 구성 요소를 구축하기 위해 증착에 의존한다는 점을 인식하세요.
- 핵심 물리 화학 이해에 중점을 둔다면: 삼중점 이하에서는 모든 거동이 직접적인 고체-기체 전환을 포함한다는 점에서 상 다이어그램을 이해의 닻으로 삼으세요.
궁극적으로 승화와 증착은 물질의 상태가 에너지와 압력의 상호 작용에 의해 지배되는 역동적인 조건임을 보여줍니다.
요약표:
| 프로세스 | 정의 | 일반적인 예시 |
|---|---|---|
| 승화 | 고체 → 기체 (직접) | 드라이아이스(고체 CO₂)가 기체로 변함 |
| 증착 | 기체 → 고체 (직접) | 차가운 창문에 서리가 맺힘 |
| 핵심 조건 | 물질의 삼중점보다 낮은 온도와 압력에서 발생 | - |
승화 및 증착에 대한 연구 또는 산업 공정을 위해 정확한 온도 및 압력 제어가 필요하십니까? KINTEK은 승화 및 증착에 필요한 조건을 안정적으로 달성하기 위해 진공 오븐 및 증착 시스템을 포함한 고성능 실험실 장비를 전문으로 합니다. 귀하의 실험실이 가진 고유한 과제에 적합한 도구를 선택하는 데 전문가들의 도움을 받으십시오. 귀하의 응용 분야에 대해 논의하려면 오늘 저희에게 연락하십시오!
시각적 가이드