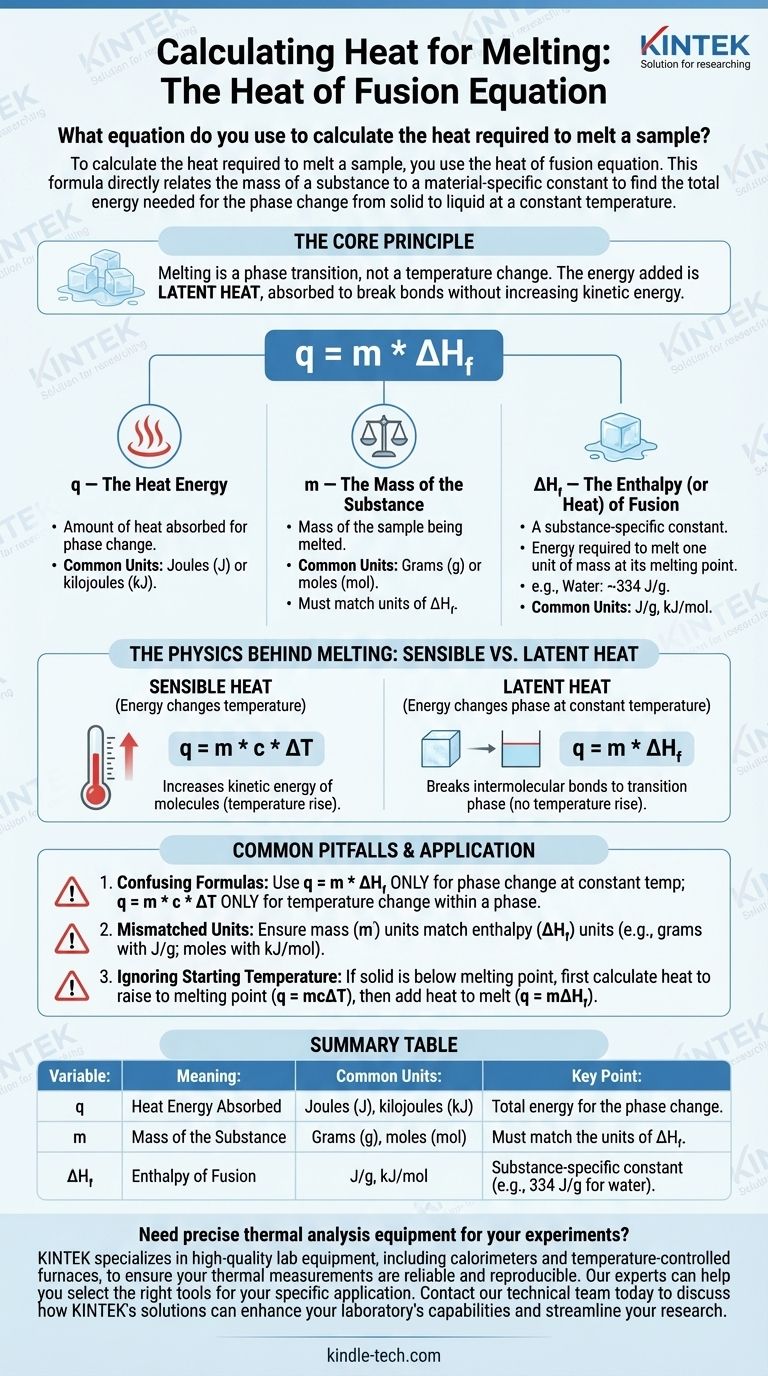
샘플을 녹이는 데 필요한 열을 계산하려면 융해열 방정식을 사용합니다. 이 공식은 물질의 질량을 물질 고유의 상수와 직접 연결하여 일정한 온도에서 고체에서 액체로 상 변화하는 데 필요한 총 에너지를 찾습니다.
핵심 원리는 녹는 것이 온도 변화가 아니라 상 전이라는 것입니다. 추가하는 에너지는 잠열이라고 불리며, 분자의 운동 에너지를 증가시키지 않고 고체 구조의 결합을 끊기 위해 흡수됩니다.
융해열 방정식 해체
녹는 동안 흡수되는 열을 계산하는 공식은 다음과 같습니다.
q = m * ΔH_f
이 방정식의 각 변수는 물리적 과정의 중요한 부분을 나타냅니다. 각각을 개별적으로 이해하는 것이 공식을 올바르게 적용하는 데 중요합니다.
q — 열에너지
q는 물질이 상 변화를 겪기 위해 흡수하는 열의 양을 나타냅니다. 이 값은 일반적으로 줄(J) 또는 킬로줄(kJ)로 표현되지만, 오래된 맥락에서는 칼로리(cal)를 사용할 수도 있습니다.
m — 물질의 질량
m은 녹이려는 샘플의 질량입니다. 질량 단위(일반적으로 그램(g) 또는 몰(mol))가 해당 물질의 융해열 상수에 사용된 단위와 일치하는 것이 중요합니다.
ΔH_f — 엔탈피(또는 열) 융해
ΔH_f는 가장 중요한 변수입니다. 이것은 융해 엔탈피이며, 종종 잠열 융해라고 불립니다.
이것은 각 물질에 고유한 물리적 상수입니다. 이는 녹는점에서 해당 물질의 단위 질량(예: 1그램 또는 1몰)을 녹이는 데 필요한 에너지 양을 정의합니다.
예를 들어, 물의 융해열은 약 그램당 334줄(J/g)입니다. 이는 0°C의 얼음 1그램을 0°C의 액체 물 1그램으로 녹이려면 334줄의 에너지를 추가해야 함을 의미합니다.

녹는 현상의 물리: 현열 vs. 잠열
녹는 동안 온도가 상승하지 않는 이유에 대한 일반적인 혼동 지점이 있습니다. 이는 두 가지 유형의 열에너지의 차이로 설명됩니다.
현열
현열은 물질의 온도를 변화시키는 에너지입니다. 현열을 추가하면 분자의 운동 에너지가 증가하여 더 빠르게 움직이게 되며, 이는 온도 상승으로 측정됩니다. 이 공식은 q = m * c * ΔT입니다.
잠열
잠열은 일정한 온도에서 상 변화 동안 흡수되거나 방출되는 에너지입니다. 녹는 동안 들어오는 에너지는 고체의 결정 격자를 함께 유지하는 분자간 결합을 끊는 데 전적으로 사용되어 액체로 전환됩니다.
에너지가 온도 상승을 유발하는 대신 상 변화에 "숨겨져" 있기 때문에 잠열이라고 불립니다.
피해야 할 일반적인 함정
잘못된 개념이나 공식을 적용하는 것은 열역학 계산에서 흔히 발생하는 오류의 원인입니다. 이러한 일반적인 실수를 인지하십시오.
융해열과 비열 혼동
가장 흔한 실수는 잘못된 공식을 사용하는 것입니다.
q = m * ΔH_f(융해열)은 일정한 온도에서 상 변화(예: 0°C에서 얼음 녹이기)에만 사용하십시오.q = m * c * ΔT(비열)은 단일 상 내에서 물질의 온도를 변경할 때만 사용하십시오(예: -10°C에서 0°C로 고체 얼음 가열하기).
단위 불일치
항상 단위를 확인하십시오. 질량(m)이 그램 단위인 경우, 융해열(ΔH_f)은 그램당 줄(J/g) 단위여야 합니다. ΔH_f가 몰당 킬로줄(kJ/mol)로 주어지면, 먼저 샘플의 질량을 몰로 변환해야 합니다.
시작 온도 무시
융해열 방정식은 물질이 이미 녹는점에 있을 때만 적용됩니다. 녹는점보다 낮은 온도의 고체가 있다면, 2단계 계산을 수행해야 합니다.
- 고체를 녹는점까지 올리는 데 필요한 열 계산(
q = mcΔT). - 녹는점에서 고체를 녹이는 데 필요한 열 계산(
q = mΔH_f). - 총 필요한 열을 얻기 위해 결과를 합산합니다.
계산에 올바른 공식 적용
문제를 올바르게 해결하려면 계산해야 할 정확한 프로세스를 식별하십시오.
- 주요 초점이 이미 녹는점에 있는 물질을 녹이는 경우: 융해열 방정식만 필요합니다:
q = m * ΔH_f. - 주요 초점이 상 변화 없이 물질을 가열하는 경우: 비열 용량 방정식만 필요합니다:
q = m * c * ΔT. - 주요 초점이 고체를 가열한 다음 완전히 녹이는 경우: 두 단계에 대한 열을 별도로 계산하여 합산해야 합니다:
q_total = (m * c * ΔT)_heating + (m * ΔH_f)_melting.
어떤 물리적 과정을 모델링하는지 이해하는 것이 올바른 방정식을 선택하는 핵심입니다.
요약표:
| 변수 | 의미 | 일반적인 단위 | 핵심 사항 |
|---|---|---|---|
| q | 흡수된 열에너지 | 줄(J), 킬로줄(kJ) | 상 변화를 위한 총 에너지 |
| m | 물질의 질량 | 그램(g), 몰(mol) | ΔH_f의 단위와 일치해야 함 |
| ΔH_f | 융해 엔탈피 | J/g, kJ/mol | 물질 고유의 상수 (예: 물의 경우 334 J/g) |
실험을 위한 정밀한 열 분석 장비가 필요하십니까?
열 요구 사항을 정확하게 계산하는 것은 재료 과학, 화학 및 제약 분야에서 필수적입니다. KINTEK은 열 측정이 신뢰할 수 있고 재현 가능하도록 열량계 및 온도 제어 용광로를 포함한 고품질 실험실 장비를 전문으로 합니다.
당사의 전문가들은 상 변화, 재료 합성 또는 반응 속도론을 연구하든 관계없이 특정 응용 분야에 적합한 도구를 선택하는 데 도움을 드릴 수 있습니다.
지금 당사 기술팀에 문의하여 KINTEK의 솔루션이 실험실의 역량을 강화하고 연구를 간소화할 수 있는 방법을 논의하십시오.
시각적 가이드